
上周,6月9日,石药集团仿制的美洛昔康注射液完成了补充资料任务,意味着不出意外,产品即将获批,美洛昔康注射液首仿即将出现。
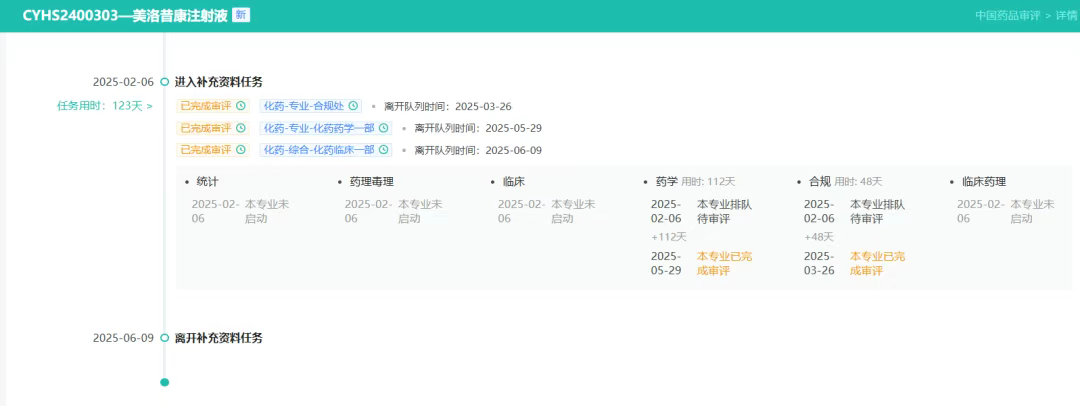
今年的5月9日,南京清普生物科技有限公司按照2.2类改良的美洛昔康注射液(Ⅱ)获批,用于成人术后疼痛管理,是国内首款长效镇痛新药。
不到两个月时间,南京清普生物就将迎来石药这一超强竞争者。
未来还有扬子江、健康元等企业在争相参与竞争,根据已有公开数据,美洛昔康注射液参与竞争企业已达8家。
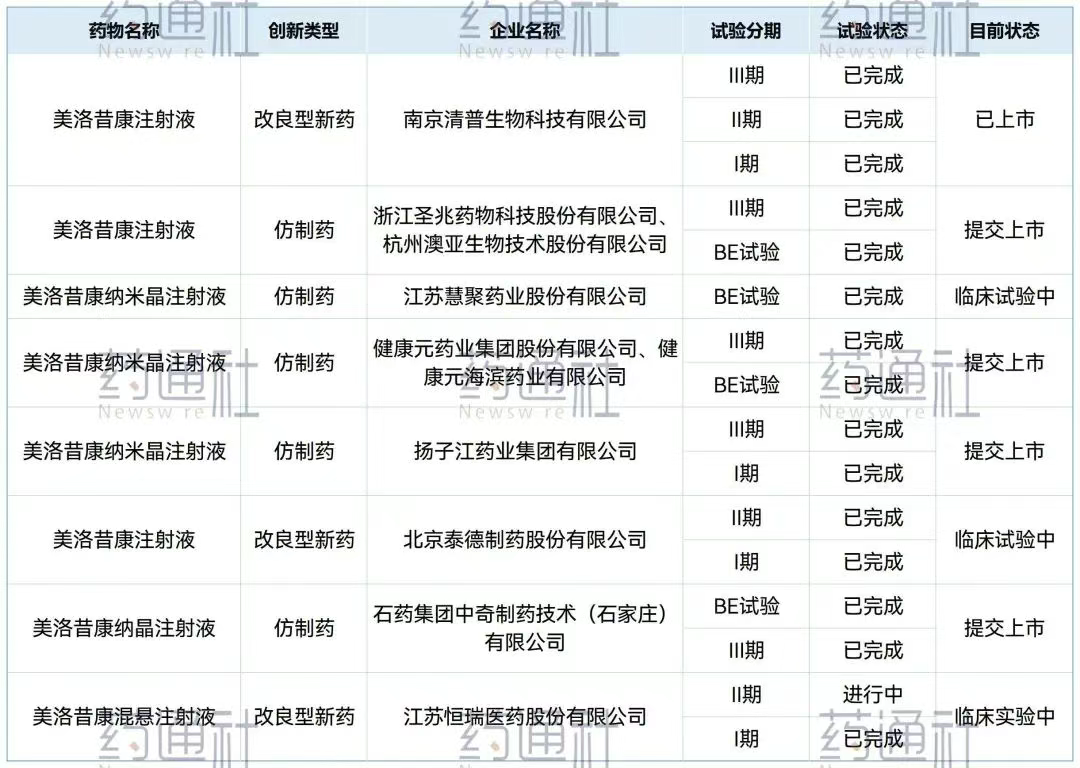
然而,美洛昔康注射液这个品种最大的争议点在于:其原研在美国已退市。
展开来说,该品原研共有两款:
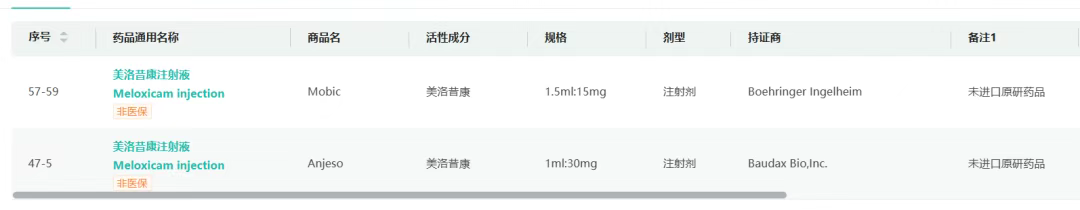
Boehringer公司的美洛昔康注射液(商品名:Mobic)给药途径为肌肉注射。Mobic虽可用于注射给药,但无法快速起效,并且使用的辅料具有刺激性和毒性,存在一定的安全性问题。
为了更进一步提高美洛昔康的止痛速度,Baudax Bio公司运用纳米晶体技术开发了美洛昔康静脉注射液(商品名:Anjeso),于2020年2月20日获FDA批准上市。
目前主流研发均是跳过Mobic,致力于仿制或改良Anjeso。
但谁曾想Anjeso命途多舛,2020年获批,2022年12月Baudax Bio公司就宣布将Anjeso退市。
Baudax Bio公司称退市是因为产品商业化不佳。
此事引发轩然大波,对预备仿制该品种的企业更是晴天霹雳,很快,仿制企业联合发起了citizen petition,FDA的回复里明确Anjeso撤市不是因为安全性和有效性原因。
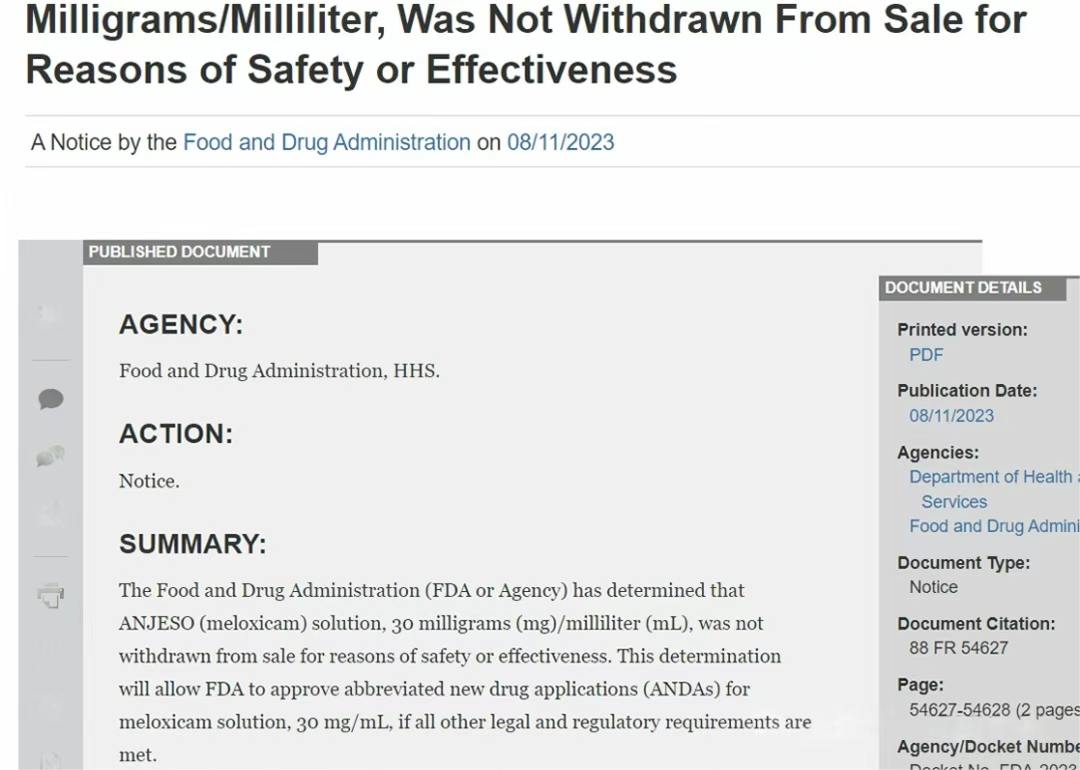
FDA的回复算是给预备仿制企业吃了一颗定心丸,但即使如此,Anjeso退市也已是不可挡的事实。
原研停产,便意味着参比不可及性大大增加。
对进行改良研究的企业无影响,但对预备仿制的企业来说就是个大问题。
石药、健康元、扬子江三家公司在2023年率先开始进行BE试验和Ⅲ期临床试验,BE试验用的参比仍旧是Anjeso。
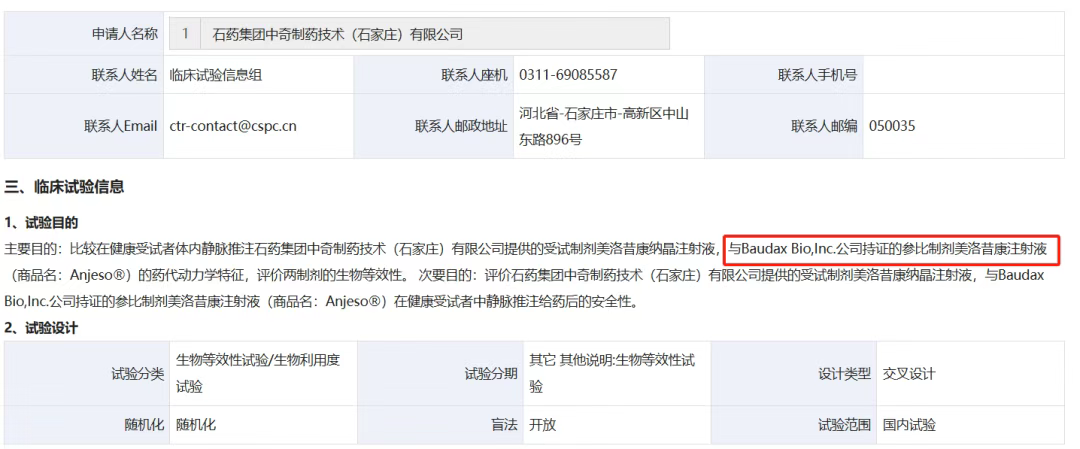
到了2024年,江苏慧聚也顺利用Anjeso完成了BE试验,这个时间点,市面上可获得的参比制剂越来越少,现存参比都快过期了。
专做复杂制剂的浙江圣兆同样在2024年进行了美洛昔康注射液的BE试验和Ⅲ期临床试验,BE试验对照用药有了变化:从Baudax Bio公司持有的美洛昔康注射液(商品名:ANJESO®)变成了Patheon Italia S.p.A.公司生产,浙江圣兆药物科技股份有限公司提供的参比制剂美洛昔康注射液(商品名:ANJESO®)
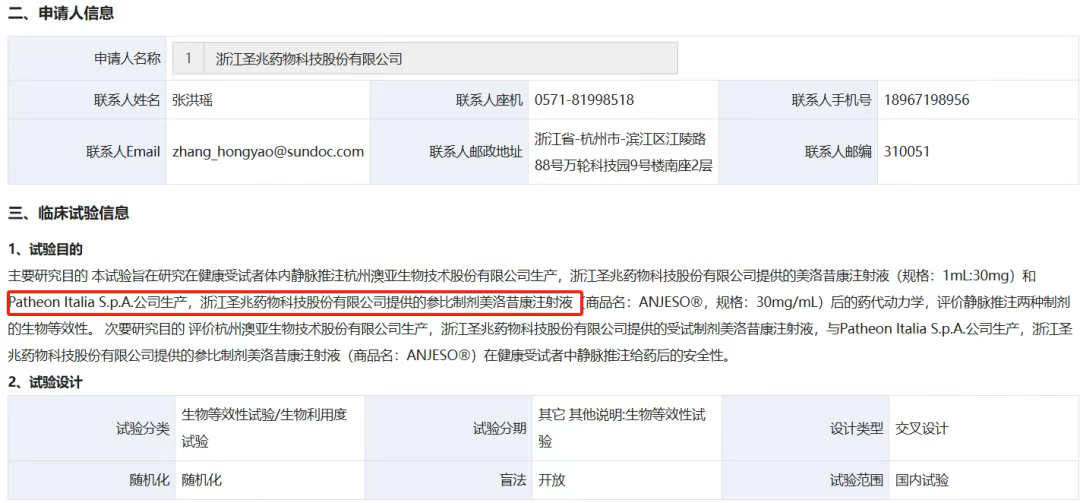
Patheon Italia S.p.A.公司似乎与Baudax Bio公司没有关联,圣兆难道为了获得参比重新找企业生产了一批Anjeso?
在有原研企业授权情况下确实可以如此操作,但耗时耗力还费钱,圣兆对美洛昔康注射液是真是势在必得了,具体情况如何圣兆未公布,但参比的难获取性可见一斑。
另外还有一点,如上文所说,原研Anjeso宣称因商业化不佳而退市,而浙江圣兆宁愿花费大量时间金钱也要仿制该产品,显然对美洛昔康注射液商业化非常有信心?
除了上述五家仿制企业,更多家企业选择在无法仿制的情况下进行改良研究。
在国内就有成功者南京清普生物科技有限公司,在恒瑞、泰德两位大佬之间突围而出,获得全球首款改良型美洛昔康注射液(Ⅱ),同时该品种也顺利在美国上市(商品名:Qamzova),目前是唯一一款中美获批上市的注射液。
6月5日,Azurity公司改良的美洛昔康注射液(商品名:Xifyrm)在美国上市,美洛昔康注射液改良后来者可不少。
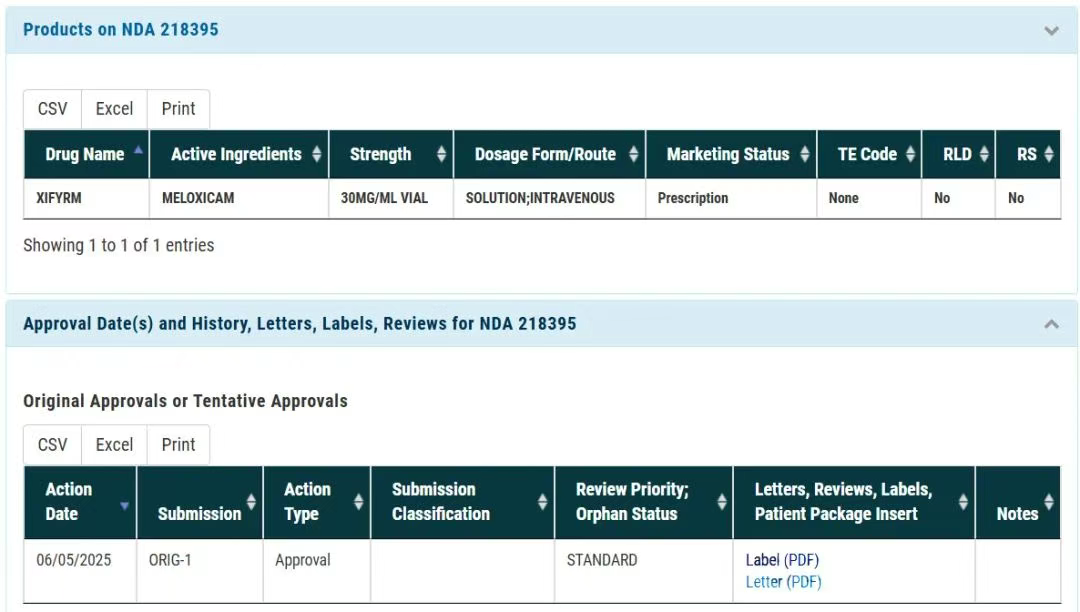
美洛昔康化合物的水溶性较低,胃肠道吸收速度缓慢,注射液研究集中在增溶,Anjeso用了纳米晶技术,南京清普采用了聚乙二醇400(PEG400)增溶技术,Azurity公司则采用的是β环糊精增溶,北京泰德已完成II期临床研究的美洛昔康注射液用的是精氨酸增溶。
美洛昔康注射液增容技术各有不同,但从现阶段来看,中美两国从未放弃过研究。
产品是否盈利最终需要上市后才能评判,相较于研发能力,企业商业化能力同样重要。
想要解锁更多药物研发信息吗?查询yl23455永利官网(原药融云)数据库(vip.sdbaichao.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!












































 浙公网安备33011002015279
浙公网安备33011002015279
 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论