
今天,CDE公布的新一批受理品种中,乙酰半胱氨酸注射液再次刷新纪录!
仅一日,就有6家企业上市申请被受理!
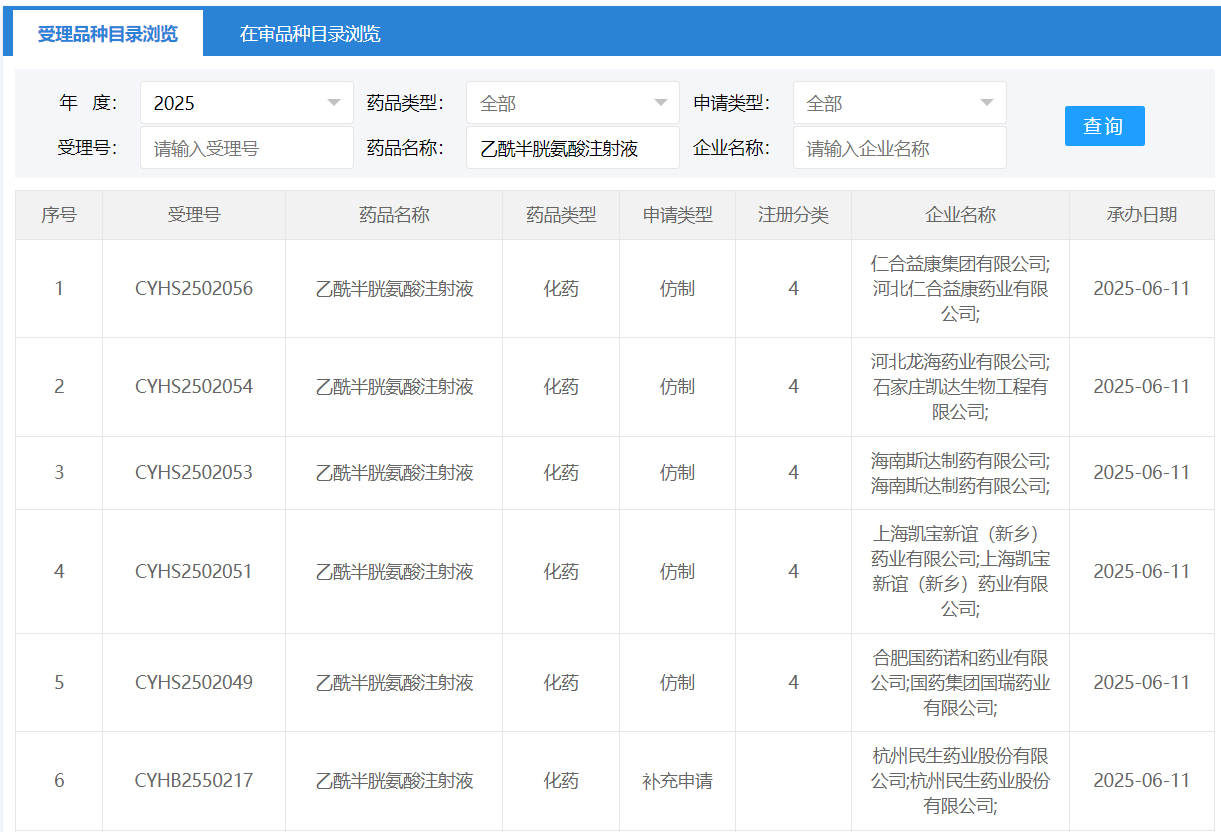
这个申报速度堪称疯狂。
自2025年5月21日赞邦原研的乙酰半胱氨酸注射液正式获批至今,仅20天时间,该品种申请上市的企业已达19家。
按目前这种速度下去,一个月突破30家不是难事。
其中,民生药业是以补充申请方式提交的一致性评价上市申请,民生药业此前拥有乙酰半胱氨酸注射液老文号(国药准字H20051788,20ml:0.4g),且市场份额超过90%,以民生所占市场份额,今日才提交上市申请,已经属于慢人一步了。
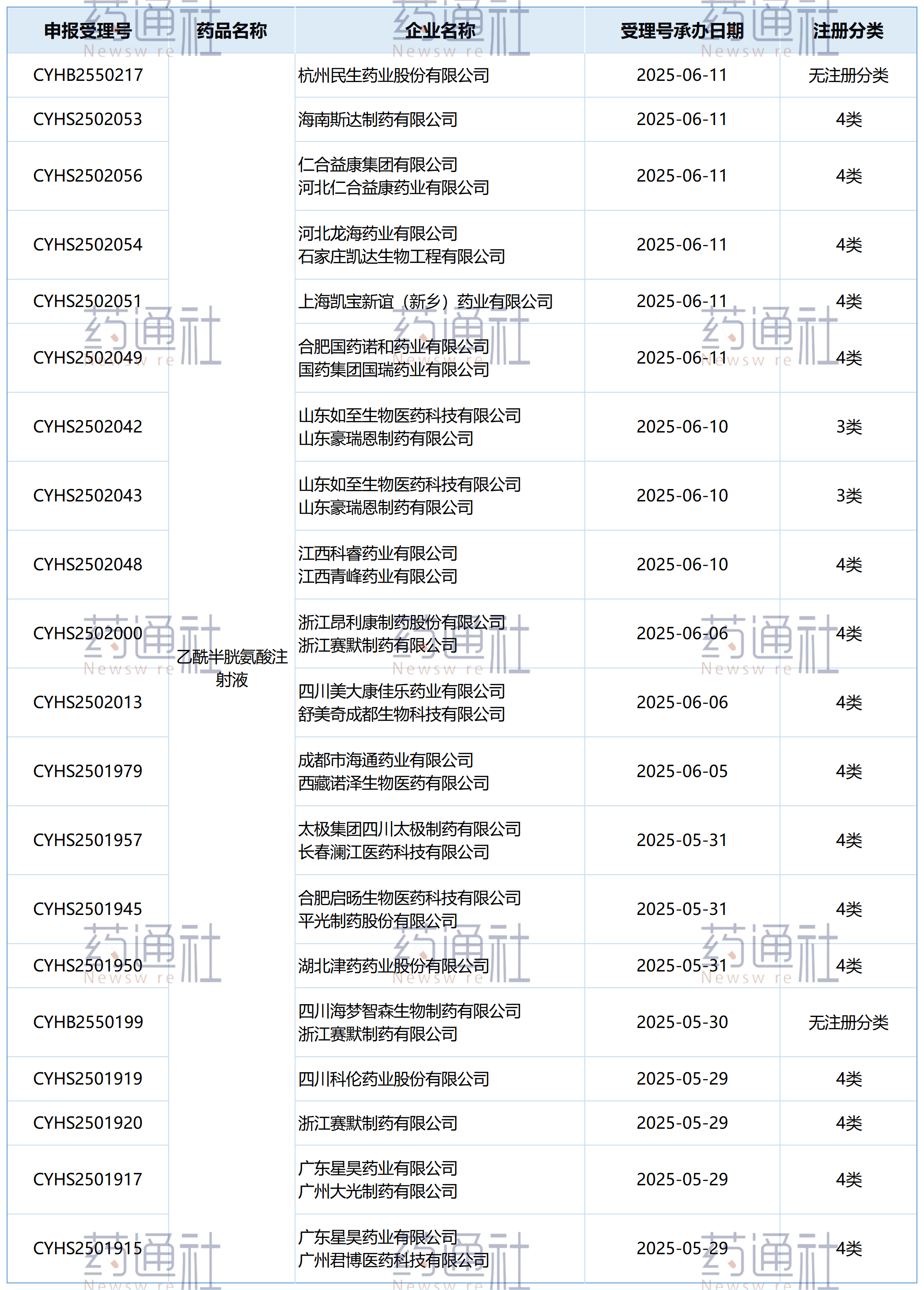
图| 5月21日后乙酰半胱氨酸注射液19家企业的上市申请
另外我们注意到,在这19家申报企业中,除民生和四川海梦为补充申请(无法查到规格)外,其余新申报企业几乎全部采用化药4类申报路径。
唯独山东如至生物医药科技有限公司,选择了化药3类。

理论上,化药3类并无问题。CDE参比制剂目录中,确实已收录了Zambon持证、尚未进口的原研药品 Flumil。
然而,在原研未上市前,已有21家国内企业以3类申报,惨遭失败。
本号也曾分析过,乙酰半胱氨酸注射液批量被驳回的原因,与适应症和规格不同有关。1个月被CDE拒批5次?规格&适应症都不太可能批准!
因此直到赞邦国内上市,行业纷纷转向4类申报,并迅速卷入激烈竞争。
所以在这样的情况下,山东如至的选择似乎有些“非常规”。
而且该企业不仅另辟蹊径以化药3类申报,还报了两个规格——20ml:4g和25ml:5g。
25ml:5g规格是Zambon国外已上市国内未上市规格;而20ml:4g规格,则是国内已有企业以保肝适应症获批的独特规格。
赞邦此次国内获批的规格为3ml:0.3g,适应症为化痰相关,目前公开可查询按照化药4类申报的企业都选择了此规格。
而山东如至选择规避这一路径,可能是试图以差异化规避竞争?
目前来看,化痰类适应症已被国内认可。那么,“相同适应症但规格不同”的情况或可获批?又或者“保肝相关适应症”也有希望顺利通过审批?
这是否会成为突破口?尚不得而知,就看审评老师如何考量了。
另外,赞邦的“富露施”已在国内上市,大批企业申报了化药4类上市,但国产“富露施”还未被遴选入参比目录,不知下一批参比意见稿里会不会出现该品种。
想要解锁更多药物研发信息吗?查询yl23455永利官网(原药融云)数据库(vip.sdbaichao.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!












































 浙公网安备33011002015279
浙公网安备33011002015279
 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论